Atom, molekül ve iyon olarak öğrendiğimiz türlerin arasında oluşan etkileşimleri anlayabilmek için bu türleri belirli ölçeklere göre sınıflandırmak gerekir.
Birinci sınıflandırma bağlanan türlerin cinsine göre yapılan sınıflandırmadır. Bu sınıflandırma atomlar arası ve moleküller arası şeklinde olmak üzere iki çeşittir. Atom ve iyon türleri arasındaki etkileşimler, atomlar arası etkileşimler; moleküller arasındaki etkileşimler de moleküller arası etkileşimler olarak tanımlanır.
Türler Arası Etkileşimler
- Atomlar Arası Etkileşimler
- Moleküller Arası Etkileşimler
Bu sınıflandırmada sodyum iyonu (Na+ ) ve klorür iyonu (Cl– ) arasında oluşan iyonik bağ, hidrojen (H) ve oksijen (O) atomları arasında oluşan kovalent bağ ve demir (Fe) atomları arasında oluşan metalik bağ atomlar arası etkileşimler olarak sınıflandırılır.
Maddenin gaz hâlinde tanecikler arası etkileşimler çok küçüktür. Bunun için asal gaz atomları arasındaki etkileşimler maddenin gaz hâlde olmasından dolayı ihmal edilir. Türler arası etkileşimlerde gaz maddeler yer almaz. Ancak bir asal gaz sıcaklığı düşürülerek sıvılaştırıldığında atomlar arasında oluşan etkileşimler moleküller arası etkileşimler sınıflandırması altında yer alır. Bunun sebebi, atomlar arası etkileşim olsa da çekim kuvvetinin çok zayıf olmasıdır.
Zayıf etkileşimler moleküller arası çekim kuvvetidir. Bu şekilde sıvı asal gaz atomları arası etkileşimler, zayıflığından dolayı moleküller arası etkileşim (London Kuvvetleri) olarak sınıflandırılır.
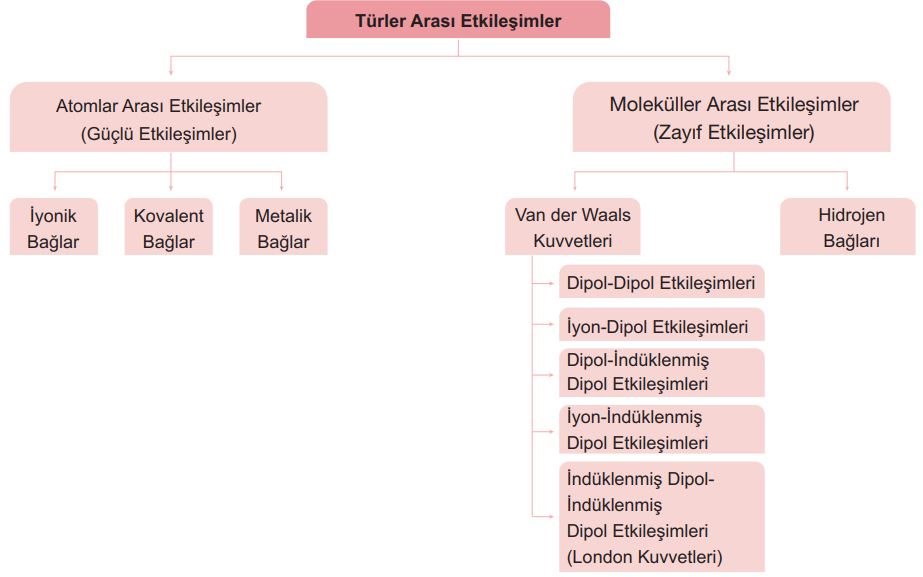
Tabloda türler arası etkileşimlerin sınıflandırılmasında güçlü ve zayıf etkileşimler ayrımı yapılmıştır. Bu sınıflandırma sonucunda iyonik bağ, kovalent bağ ve metalik bağ güçlü etkileşimler, hidrojen bağı ve Van der Waals kuvvetleri ise zayıf etkileşimlerdir.
Güçlü etkileşimler kimyasal bağlardır. Kopmaları veya oluşmaları sırasında oluşan enerji değişimi büyüktür. Zayıf etkileşimler ise fiziksel çekim kuvvetleridir. Bunlar kimyasal bağ olarak tanımlanamaz. Kopmaları veya oluşmaları sırasında alınan veya verilen enerji değerleri genelde küçüktür.
Sonuç olarak kimyasal bağlar (güçlü etkileşimler) koptuğunda ve oluştuğunda yeni kimyasal türler meydana gelir ve maddenin kimlik özellikleri değişir. Fiziksel çekim kuvvetleri (zayıf etkileşimler) oluştuğunda veya koptuğunda ise kimyasal türlerde bir değişiklik olmaz. Sadece maddenin fiziksel hâlinde bir değişme olur, kimlik özellikleri değişmez.
Sıvı azot oda sıcaklığında kendiliğinden kaynayarak gaz hâline geçer. Bu sırada maddenin N2 (s) olarak gösterilen kimyasal yapısında bir değişim olmaz. Sadece N2 (s) molekülleri arasındaki etkileşimlerin maddenin gaz hâle geçmesinden dolayı koptuğu kabul edilir. Bu olayda fiziksel çekim kuvvetleri kopmuştur.
Bir uzay aracındaki yanma tepkimeleri sonucunda çok büyük enerji açığa çıkar. Oluşan yanma tepkimesi sonucunda kimyasal türler parçalanır ve yeni türler oluşur. Bu değişimler sırasında kimyasal bağlar (güçlü etkileşimler) kopar ve yeni kimyasal bağlar oluşur.
